مقدمه
زبرافیش (Danio rerio) یا گورخرماهی بهعنوان یک مدل مهرهدار برجسته در تحقیقات زیستپزشکی، بهویژه در فارماکولوژی و سمشناسی شناخته شده است. اندازه کوچک، رشد سریع و لقاح خارجی آنها را برای مطالعات درونتن بسیار مناسب کرده است. جنینها و لاروهای زبرافیش شفاف هستند و امکان تصویربرداری زنده از رفتار دارو در بدن موجود زنده را فراهم میکنند. جنینها خارج از بدن مادر رشد میکنند و در مدت کوتاهی بالغ میشوند، که امکان غربالگری سریع ترکیبات را فراهم میسازد. همچنین، به دلیل زیست این موجودات در آب، امکان دارورسانی از طریق آب، تزریق یا میکروتزریق در آنها وجود دارد و هزینه نگهداری آنها را کاهش میدهد.

شکل 1 زبرافیش یا گورخر ماهی وحشی
از نظر ژنتیکی، زبرافیش حدود 70% مشابهت ژنتیکی با انسان دارد. بسیاری از ژنهای دخیل در متابولیسم و انتقال دارو مانند آنزیمهای CYP450، UGT و P-gp، میان انسان و زبرافیش مشترک هستند که زبرافیش را به مدلی با قابلیت تعمیم مناسب به انسان تبدیل کرده است.
در فارماکوکینتیک، درک نحوه جذب، توزیع، متابولیسم و دفع دارو (ADME) برای پیشبینی اثربخشی و ایمنی دارو ضروری است. زبرافیش بستری منحصربهفرد برای مطالعه این فرآیندها در سطح کل موجود زنده (whole organism) فراهم میکند و شکاف میان آزمونهای سلولی و مدلهای پستانداری را پر میسازد.
مطالعات جذب در زبرافیش
جذب دارو در لاروهای زبرافیش از مسیرهای مختلفی از جمله جذب پوستی، جذب از طریق آبشش، جذب گوارشی (4 تا 5 روز پس از لقاح) و تزریق مستقیم انجام میشود. رایجترین روش، غوطهوری در محیط دارویی است که در آن، دارو در محیط کشت ماهی حل میشود. با این حال، کارایی جذب بهشدت به ویژگیهای فیزیکوشیمیایی دارو بستگی دارد.
مطالعاتی با استفاده از رنگهای فلورسانس با LogD متفاوت نشان دادهاند که ترکیبات لیپوفیلیک مانند CY3A (LogD = 1.73) از طریق غوطهوری بهخوبی جذب میشوند، در حالیکه ترکیبات هیدروفیلیک نیاز به تزریق مستقیم دارند. Guarin و همکاران نشان دادند که تزریق داخلصفاقی و پریکاردی، بهویژه در دورههای درمانی کوتاهمدت، باعث جذب سریعتر و یکنواختتر نسبت به غوطهوری میشود.
لاروهای زبرافیش بین روزهای ۳ تا ۵ پس از لقاح دچار بلوغ فیزیولوژیکی میشوند که بر جذب و دفع دارو تأثیر میگذارد. Van Wijk و همکاران جذب استامینوفن را در لاروهای زبرافیش اندازهگیری کردند و دریافتند که نرخ جذب بین روزهای ۳ تا ۴ پس از لقاح دو برابر میشود که به باز شدن دستگاه گوارش مربوط است. دفع روزانه نیز ۱۷.5% افزایش داشت. بنابراین، توصیه میشود مطالعات فارماکوکینتیک در روز پنجم پس از لقاح انجام شوند.

شکل 2 لاروهای 5 روزه زبرافیش.
مطالعات توزیع در زبرافیش
شفافیت لاروهای زبرافیش امکان مشاهده مستقیم محل تجمع دارو را با استفاده از نشانگرهای فلورسانس فراهم میکند. تصویربرداری با میکروسکوپ کانفوکال و طیفسنجی جرمی برای ردیابی توزیع دارو در اندامهایی مانند کبد، مغز و قلب استفاده شده است. برای مثال، Kulkarni و همکاران نفوذ دارو به مغز را در زبرافیش بالغ بررسی کردند و دریافتند که پروفایل فارماکوکینتیک با پستانداران، از جمله انسان، همخوانی دارد.
تزریق مستقیم به حفره پریکارد یا صفاقی نیز امکان مطالعه توزیع بافتی بدون عبور از موانع جذب را فراهم میکند. ترکیب غوطهوری با تزریق باعث افزایش و تثبیت سطح درونتن دارو در طول زمان میشود.
مطالعات متابولیسم در زبرافیش
زبرافیش دارای آنزیمهای کلیدی متابولیسم مانند CYP450، UGT و SULT است که در مهرهداران نیز حفظ شدهاند. مطالعات متعددی متابولیسم استامینوفن را در زبرافیش بررسی کردهاند. مطالعات نشان دادهاند که در زبرافیش استامینوفن عمدتاً با گروههای سولفات کانژوگه میشود، که مشابه متابولیسم نوزاد انسان است. این نشان میدهد که زبرافیش میتواند مدل مناسبی برای بررسی متابولیسم وابسته به سن باشد.
زبرافیش همچنین برای بررسی متابولیسم داروهای ضدسرطان، مواد مخدر و آلایندههای محیطی استفاده شده است. ظرفیت متابولیکی زبرافیش با افزایش سن افزایش مییابد، بنابراین لاروهای پنج روزه برای مطالعات متابولیسم نیز مناسبتر هستند.
شکل 3 لارو شفاف زبرافیش از نمای نزدیک.
مطالعات دفع در زبرافیش
دفع آخرین مرحله در حذف دارو از بدن است و شامل دفع از طریق آبشش، کلیه، کبد و روده میشود. اندازه کوچک زبرافیش امکان آنالیز کل بدن و اندازهگیری متابولیتهای دفعشده را فراهم میکند.
در مطالعات مختلفی استامینوفن و متابولیتهای آن را در لاروهای هموژنشده و محیط اطراف آنها اندازهگیری و کلیرانس مطلق را محاسبه کردهاند. نشان داده شده است که کلیرانس با افزایش سن افزایش مییابد که میتواند با بلوغ اندامهای دفعی مرتبط باشد. مطالعات بر روی ترکیبات فلورسانس نشان دادهاند که مواد زیستفعال و متابولیتها از طریق کلواک (مخرج مشترک مجاری گوارشی، ادراری و تناسلی) دفع میشوند و ترکیبات چربیدوست نیمهعمر طولانیتری دارند. علاوه بر این، مطالعات دفع با استفاده از تصویربرداری و طیفسنجی جرمی امکان ردیابی حذف دارو در طول زمان را فراهم میکنند و برای درک ماندگاری دارو و خطرات سمیت بسیار مهم هستند.
ترجمه نتایج مدل زبرافیش به سایر پستانداران و انسان
نتایج بهدستآمده در مدل زبرافیش معمولاً بهصورت نسبی و در چارچوبهای مقایسهای به سایر پستانداران و انسان قابل تعمیم هستند؛ نه بهصورت مستقیم و یکبهیک. لارو زبرافیش بهعنوان یک مدل میانجی بین آزمایشهای سلولی و مدلهای پستانداری عمل میکند و میتواند روندهای کلی مانند جذب از محیط، توزیع بافتی بالقوه، مسیرهای متابولیکی غالب و الگوهای اولیه دفع را نشان دهد. این اطلاعات به خصوص در مرحله انتخاب اولیه ترکیبات و شناسایی مکانیسمها ارزشمند است، اما برای پیشبینی کمی و دقیق پارامترهایی مثل AUC یا کلیرانس لازم است از روشهای مدلسازی ترجمهای (مانند IVIVE یا مدلهای مکانیسمی فیزیولوژیک) استفاده شود و یافتههای زبرافیش با دادههای پستانداران مقایسه و کالیبره شود.
چند عامل محدودکننده برای قابلیت تعمیم نتایج به دست آمده از مدل زبرافیش وجود دارد که شامل تفاوت در فنوتیپهای آنزیمی (مانند الگوها و سطح بیان آنزیمهای دخیل در متابولیسم)، تکوین ناکامل اندامها در مراحل اولیه نمو و تفاوتهای فیزیولوژیک مثل ساختار پوست، آبشش و مسیرهای دفع میشود. وقتی همبستگیهای سیستماتیک بین پارامترهای کلیدی در زبرافیش و گونههای پستاندار نشان داده و کمیسازی شود، میتوان پیشبینیهایی محتاطانه برای انسان ارائه کرد؛ اما این پیشبینیها همیشه همراه با بازههای عدمقطعیت و نیازمند اعتبارسنجی تجربی در مدلهای پستاندار خواهد بود.
در عمل، بهترین رویکرد به صورت ترکیبی است؛ استفاده از زبرافیش برای غربالگری عملکردی، شناسایی مسیرهای متابولیک و تعیین جهتگیری اولیه PK/PD؛ و سپس بهرهگیری از دادههای زبرافیش در مدلهای کمی برای طراحی مطالعات مدلهای پستاندار هدفمند و کاهش تعداد آزمایشات بزرگتر. پذیرش نهایی و استفاده از پیشبینیها در شرایط بالینی مستلزم نشان دادن انطباق آماری و بیولوژیک بین نتایج زبرافیش و دادههای مرجع پستانداران/انسان است، و این موضوع همچنان موضوعی فعال در تحقیقات ترجمهای است.
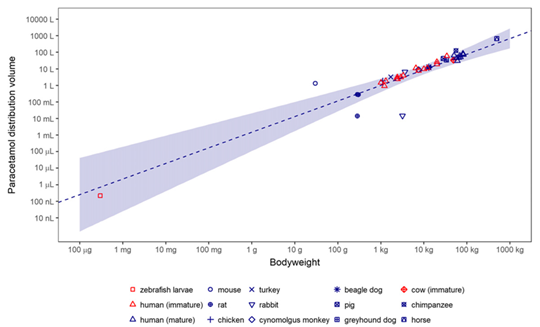
شکل 4 ارتباط میان حجم توزیع استامینوفن در زبرافیش با سایر مدل های حیوانی و انسان.
زبرافیش از منظر نهادهای نظارتی
سازمانهایی مانند FDA و EMA هنوز زبرافیش را بهعنوان مدل اصلی برای مطالعات فارماکوکینتیک در پروندههای IND یا NDA نمیپذیرند. مدلهای پستانداری همچنان مرجع اصلی برای ارزیابیهای پیشبالینی هستند. با این حال، زبرافیش بهعنوان مدل مکمل در مراحل اکتشافی مورد پذیرش قرار گرفته است. قانون FDA Modernization Act 2.0 که در سال ۲۰۲۲ تصویب شد، استفاده از مدلهای جایگزین حیوانی از جمله زبرافیش را تشویق میکند. این مدل با اصول 3R (جایگزینی (Replacement)، کاهش (Reduction)، پالایش (Refinement)) همراستا است. راهنماهای نظارتی مانند ICH M3(R2) و اسناد بازتابی EMA به نقش مدلهای جایگزین در آزمونهای یکپارچه (integrated) اشاره دارند.

شکل 5 زیرگونه Casper زبرافیش که پس از بلوغ نیز شفاف باقی میماند.
جمعبندی
زبرافیش با ترکیب منحصربهفردی از شباهت ژنتیکی، انعطافپذیری آزمایشگاهی و قابلیت تصویربرداری زنده، جایگاه ویژهای در پژوهشهای فارماکوکینتیک یافته است. اگرچه هنوز بهعنوان مدل اصلی در مطالعات فارماکوکینتیک مورد تأیید سازمانهای نظارتی نیست، اما نقش آن در غربالگری اولیه و ارزیابی سمیت غیرقابل انکار است. با تحول در سیاستهای نظارتی و پذیرش مدلهای جایگزین، زبرافیش میتواند نقش پررنگتری در فارماکولوژی ترجمهای (translational pharmacology) ایفا کند. ادغام دادههای زبرافیش با مدلهای پستاندار و شبیهسازیهای رایانهای، مسیر توسعه دارو را تسریع خواهد کرد و پلی میان پژوهشهای آزمایشگاهی و کاربرد بالینی خواهد ساخت. با تحول در سیاستهای نظارتی و پذیرش مدلهای جایگزین، زبرافیش نقش پررنگتری در توسعه دارو، فارماکولوژی ترجمهای و فارماکوکینتیک به دست خواهد آورد.
منابع
در فارماکوکینتیک، درک نحوه جذب، توزیع، متابولیسم و دفع دارو (ADME) برای پیشبینی اثربخشی و ایمنی دارو ضروری است. زبرافیش بستری منحصربهفرد برای مطالعه این فرآیندها در سطح کل موجود زنده (whole organism) فراهم میکند و شکاف میان آزمونهای سلولی و مدلهای پستانداری را پر میسازد.
مطالعات جذب در زبرافیش
جذب دارو در لاروهای زبرافیش از مسیرهای مختلفی از جمله جذب پوستی، جذب از طریق آبشش، جذب گوارشی (4 تا 5 روز پس از لقاح) و تزریق مستقیم انجام میشود. رایجترین روش، غوطهوری در محیط دارویی است که در آن، دارو در محیط کشت ماهی حل میشود. با این حال، کارایی جذب بهشدت به ویژگیهای فیزیکوشیمیایی دارو بستگی دارد.
مطالعاتی با استفاده از رنگهای فلورسانس با LogD متفاوت نشان دادهاند که ترکیبات لیپوفیلیک مانند CY3A (LogD = 1.73) از طریق غوطهوری بهخوبی جذب میشوند، در حالیکه ترکیبات هیدروفیلیک نیاز به تزریق مستقیم دارند. Guarin و همکاران نشان دادند که تزریق داخلصفاقی و پریکاردی، بهویژه در دورههای درمانی کوتاهمدت، باعث جذب سریعتر و یکنواختتر نسبت به غوطهوری میشود.
لاروهای زبرافیش بین روزهای ۳ تا ۵ پس از لقاح دچار بلوغ فیزیولوژیکی میشوند که بر جذب و دفع دارو تأثیر میگذارد. Van Wijk و همکاران جذب استامینوفن را در لاروهای زبرافیش اندازهگیری کردند و دریافتند که نرخ جذب بین روزهای ۳ تا ۴ پس از لقاح دو برابر میشود که به باز شدن دستگاه گوارش مربوط است. دفع روزانه نیز ۱۷.5% افزایش داشت. بنابراین، توصیه میشود مطالعات فارماکوکینتیک در روز پنجم پس از لقاح انجام شوند.

شکل 2 لاروهای 5 روزه زبرافیش.
مطالعات توزیع در زبرافیش
شفافیت لاروهای زبرافیش امکان مشاهده مستقیم محل تجمع دارو را با استفاده از نشانگرهای فلورسانس فراهم میکند. تصویربرداری با میکروسکوپ کانفوکال و طیفسنجی جرمی برای ردیابی توزیع دارو در اندامهایی مانند کبد، مغز و قلب استفاده شده است. برای مثال، Kulkarni و همکاران نفوذ دارو به مغز را در زبرافیش بالغ بررسی کردند و دریافتند که پروفایل فارماکوکینتیک با پستانداران، از جمله انسان، همخوانی دارد.
تزریق مستقیم به حفره پریکارد یا صفاقی نیز امکان مطالعه توزیع بافتی بدون عبور از موانع جذب را فراهم میکند. ترکیب غوطهوری با تزریق باعث افزایش و تثبیت سطح درونتن دارو در طول زمان میشود.
مطالعات متابولیسم در زبرافیش
زبرافیش دارای آنزیمهای کلیدی متابولیسم مانند CYP450، UGT و SULT است که در مهرهداران نیز حفظ شدهاند. مطالعات متعددی متابولیسم استامینوفن را در زبرافیش بررسی کردهاند. مطالعات نشان دادهاند که در زبرافیش استامینوفن عمدتاً با گروههای سولفات کانژوگه میشود، که مشابه متابولیسم نوزاد انسان است. این نشان میدهد که زبرافیش میتواند مدل مناسبی برای بررسی متابولیسم وابسته به سن باشد.
زبرافیش همچنین برای بررسی متابولیسم داروهای ضدسرطان، مواد مخدر و آلایندههای محیطی استفاده شده است. ظرفیت متابولیکی زبرافیش با افزایش سن افزایش مییابد، بنابراین لاروهای پنج روزه برای مطالعات متابولیسم نیز مناسبتر هستند.

شکل 3 لارو شفاف زبرافیش از نمای نزدیک.
مطالعات دفع در زبرافیش
دفع آخرین مرحله در حذف دارو از بدن است و شامل دفع از طریق آبشش، کلیه، کبد و روده میشود. اندازه کوچک زبرافیش امکان آنالیز کل بدن و اندازهگیری متابولیتهای دفعشده را فراهم میکند.
در مطالعات مختلفی استامینوفن و متابولیتهای آن را در لاروهای هموژنشده و محیط اطراف آنها اندازهگیری و کلیرانس مطلق را محاسبه کردهاند. نشان داده شده است که کلیرانس با افزایش سن افزایش مییابد که میتواند با بلوغ اندامهای دفعی مرتبط باشد. مطالعات بر روی ترکیبات فلورسانس نشان دادهاند که مواد زیستفعال و متابولیتها از طریق کلواک (مخرج مشترک مجاری گوارشی، ادراری و تناسلی) دفع میشوند و ترکیبات چربیدوست نیمهعمر طولانیتری دارند. علاوه بر این، مطالعات دفع با استفاده از تصویربرداری و طیفسنجی جرمی امکان ردیابی حذف دارو در طول زمان را فراهم میکنند و برای درک ماندگاری دارو و خطرات سمیت بسیار مهم هستند.
ترجمه نتایج مدل زبرافیش به سایر پستانداران و انسان
نتایج بهدستآمده در مدل زبرافیش معمولاً بهصورت نسبی و در چارچوبهای مقایسهای به سایر پستانداران و انسان قابل تعمیم هستند؛ نه بهصورت مستقیم و یکبهیک. لارو زبرافیش بهعنوان یک مدل میانجی بین آزمایشهای سلولی و مدلهای پستانداری عمل میکند و میتواند روندهای کلی مانند جذب از محیط، توزیع بافتی بالقوه، مسیرهای متابولیکی غالب و الگوهای اولیه دفع را نشان دهد. این اطلاعات به خصوص در مرحله انتخاب اولیه ترکیبات و شناسایی مکانیسمها ارزشمند است، اما برای پیشبینی کمی و دقیق پارامترهایی مثل AUC یا کلیرانس لازم است از روشهای مدلسازی ترجمهای (مانند IVIVE یا مدلهای مکانیسمی فیزیولوژیک) استفاده شود و یافتههای زبرافیش با دادههای پستانداران مقایسه و کالیبره شود.
چند عامل محدودکننده برای قابلیت تعمیم نتایج به دست آمده از مدل زبرافیش وجود دارد که شامل تفاوت در فنوتیپهای آنزیمی (مانند الگوها و سطح بیان آنزیمهای دخیل در متابولیسم)، تکوین ناکامل اندامها در مراحل اولیه نمو و تفاوتهای فیزیولوژیک مثل ساختار پوست، آبشش و مسیرهای دفع میشود. وقتی همبستگیهای سیستماتیک بین پارامترهای کلیدی در زبرافیش و گونههای پستاندار نشان داده و کمیسازی شود، میتوان پیشبینیهایی محتاطانه برای انسان ارائه کرد؛ اما این پیشبینیها همیشه همراه با بازههای عدمقطعیت و نیازمند اعتبارسنجی تجربی در مدلهای پستاندار خواهد بود.
در عمل، بهترین رویکرد به صورت ترکیبی است؛ استفاده از زبرافیش برای غربالگری عملکردی، شناسایی مسیرهای متابولیک و تعیین جهتگیری اولیه PK/PD؛ و سپس بهرهگیری از دادههای زبرافیش در مدلهای کمی برای طراحی مطالعات مدلهای پستاندار هدفمند و کاهش تعداد آزمایشات بزرگتر. پذیرش نهایی و استفاده از پیشبینیها در شرایط بالینی مستلزم نشان دادن انطباق آماری و بیولوژیک بین نتایج زبرافیش و دادههای مرجع پستانداران/انسان است، و این موضوع همچنان موضوعی فعال در تحقیقات ترجمهای است.

شکل 4 ارتباط میان حجم توزیع استامینوفن در زبرافیش با سایر مدل های حیوانی و انسان.
زبرافیش از منظر نهادهای نظارتی
سازمانهایی مانند FDA و EMA هنوز زبرافیش را بهعنوان مدل اصلی برای مطالعات فارماکوکینتیک در پروندههای IND یا NDA نمیپذیرند. مدلهای پستانداری همچنان مرجع اصلی برای ارزیابیهای پیشبالینی هستند. با این حال، زبرافیش بهعنوان مدل مکمل در مراحل اکتشافی مورد پذیرش قرار گرفته است. قانون FDA Modernization Act 2.0 که در سال ۲۰۲۲ تصویب شد، استفاده از مدلهای جایگزین حیوانی از جمله زبرافیش را تشویق میکند. این مدل با اصول 3R (جایگزینی (Replacement)، کاهش (Reduction)، پالایش (Refinement)) همراستا است. راهنماهای نظارتی مانند ICH M3(R2) و اسناد بازتابی EMA به نقش مدلهای جایگزین در آزمونهای یکپارچه (integrated) اشاره دارند.

شکل 5 زیرگونه Casper زبرافیش که پس از بلوغ نیز شفاف باقی میماند.
جمعبندی
زبرافیش با ترکیب منحصربهفردی از شباهت ژنتیکی، انعطافپذیری آزمایشگاهی و قابلیت تصویربرداری زنده، جایگاه ویژهای در پژوهشهای فارماکوکینتیک یافته است. اگرچه هنوز بهعنوان مدل اصلی در مطالعات فارماکوکینتیک مورد تأیید سازمانهای نظارتی نیست، اما نقش آن در غربالگری اولیه و ارزیابی سمیت غیرقابل انکار است. با تحول در سیاستهای نظارتی و پذیرش مدلهای جایگزین، زبرافیش میتواند نقش پررنگتری در فارماکولوژی ترجمهای (translational pharmacology) ایفا کند. ادغام دادههای زبرافیش با مدلهای پستاندار و شبیهسازیهای رایانهای، مسیر توسعه دارو را تسریع خواهد کرد و پلی میان پژوهشهای آزمایشگاهی و کاربرد بالینی خواهد ساخت. با تحول در سیاستهای نظارتی و پذیرش مدلهای جایگزین، زبرافیش نقش پررنگتری در توسعه دارو، فارماکولوژی ترجمهای و فارماکوکینتیک به دست خواهد آورد.
منابع
1. Van Wijk et al. (2019). Mechanistic and Quantitative Understanding of Pharmacokinetics in Zebrafish Larvae. J Pharmacol Exp Ther, 371:15–24. https://doi.org/10.1124/jpet.119.2602992
2.Kantae et al. (2016). Pharmacokinetic Modeling of Paracetamol in Zebrafish Larvae. Zebrafish, 13(6):504–509. https://doi.org/10.1089/zeb.2016.1313
3.Guarin et al. (2021). Pharmacokinetics in Zebrafish Embryos Following Immersion and Intrayolk Administration. Pharmaceuticals, 14(6):576. https://doi.org/10.3390/ph14060576
4.Guarin et al. (2025). Spatiotemporal Imaging and Pharmacokinetics of Fluorescent Compounds in Zebrafish. Scientific Reports, 11:12229. https://doi.org/10.1038/s41598-021-91612-6
5.Kulkarni et al. (2017). Correlation of Pharmacokinetics and Brain Penetration in Zebrafish and Mammals. J Pharmacol Toxicol Methods. https://doi.org/10.1016/j.vascn.2017.09.258
6.Transcending authorship. Translational pharmacokinetics-pharmacodynamics in zebrafish larvae. Universiteitleiden; [Accessed online]. https://scholarlypublications.universiteitleiden.nl/access/item%3A2984103/view
7.Howe M, Anderson J, et al. Testing the Translational Power of the Zebrafish: An Overview. Front Pharmacol. 2019;10:893. https://doi.org/10.3389/fphar.2019.00893
2.Kantae et al. (2016). Pharmacokinetic Modeling of Paracetamol in Zebrafish Larvae. Zebrafish, 13(6):504–509. https://doi.org/10.1089/zeb.2016.1313
3.Guarin et al. (2021). Pharmacokinetics in Zebrafish Embryos Following Immersion and Intrayolk Administration. Pharmaceuticals, 14(6):576. https://doi.org/10.3390/ph14060576
4.Guarin et al. (2025). Spatiotemporal Imaging and Pharmacokinetics of Fluorescent Compounds in Zebrafish. Scientific Reports, 11:12229. https://doi.org/10.1038/s41598-021-91612-6
5.Kulkarni et al. (2017). Correlation of Pharmacokinetics and Brain Penetration in Zebrafish and Mammals. J Pharmacol Toxicol Methods. https://doi.org/10.1016/j.vascn.2017.09.258
6.Transcending authorship. Translational pharmacokinetics-pharmacodynamics in zebrafish larvae. Universiteitleiden; [Accessed online]. https://scholarlypublications.universiteitleiden.nl/access/item%3A2984103/view
7.Howe M, Anderson J, et al. Testing the Translational Power of the Zebrafish: An Overview. Front Pharmacol. 2019;10:893. https://doi.org/10.3389/fphar.2019.00893
